สารบัญ
ในวิชาเคมี คำว่า จุดเดือด หมายถึง อุณหภูมิที่ของเหลวเปลี่ยนสถานะเป็นแก๊ส โดยความดันไอของของเหลวมีค่าเท่ากับความดันภายนอก
คำถามสำคัญที่เจอในห้องเรียนและข้อสอบคือ
ทำไมสารแต่ละชนิดถึงมีจุดเดือดไม่เท่ากัน?
พี่ปีโป้จะพาไล่คิดแบบเป็นระบบ ไม่ต้องท่องจำ แต่เข้าใจจาก “เหตุผลทางเคมี” จริง ๆ
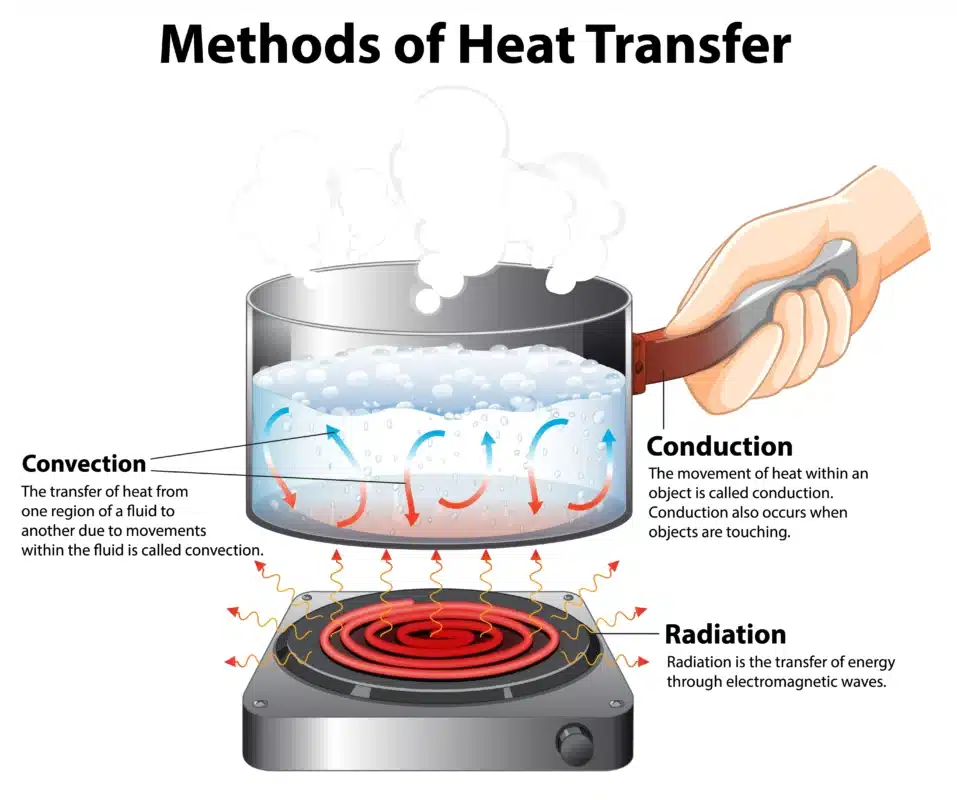
สาเหตุหลักที่ทำให้ “จุดเดือดไม่เท่ากัน”
1. แรงยึดเหนี่ยวระหว่างโมเลกุล (Intermolecular Forces)
ยิ่งแรงยึดเหนี่ยวระหว่างโมเลกุล แข็งแรงมากเท่าไร
→ ต้องใช้พลังงานมาก
→ จุดเดือดสูงขึ้น
ตัวอย่างแรงยึดเหนี่ยว
- Hydrogen Bond (แรงมาก)
- Dipole–Dipole
- London Dispersion Force (แรงอ่อน)
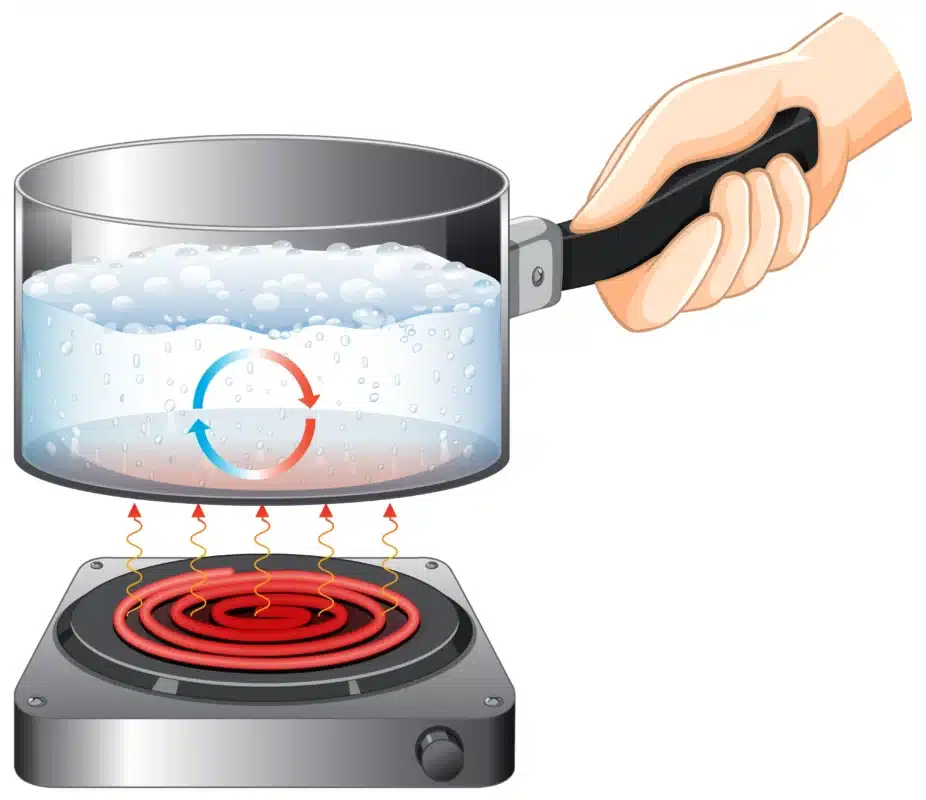
2. มวลโมเลกุล (Molecular Mass)
- มวลมาก → แรงลอนดอนมากขึ้น → จุดเดือดสูงขึ้น
- แต่ต้องดู “โครงสร้าง” ร่วมด้วย ไม่ใช่ดูมวลอย่างเดียว
3. รูปร่างโมเลกุล (Molecular Shape)
- โมเลกุลที่เป็นเส้นยาว สัมผัสกันได้มาก → จุดเดือดสูง
- โมเลกุลแตกแขนงมาก → สัมผัสน้อย → จุดเดือดต่ำ
ตารางเปรียบเทียบ: ทำไมสารใกล้เคียงกัน แต่จุดเดือดต่างกัน
| สาร | แรงยึดเหนี่ยวหลัก | จุดเดือด (°C) | วิเคราะห์แบบพี่ปีโป้ |
|---|---|---|---|
| H₂O | Hydrogen Bond | 100 | แรงยึดเหนี่ยวสูงมาก |
| H₂S | Dipole–Dipole | -60 | ไม่มี H-bond |
| CH₄ | London Force | -161 | โมเลกุลเล็ก แรงอ่อน |
| C₂H₆ | London Force | -89 | มวลมากขึ้น จุดเดือดสูงกว่า CH₄ |
ตารางนี้เป็นแนวคิดที่ “ออกสอบบ่อยมาก” โดยเฉพาะข้อเปรียบเทียบเชิงเหตุผล
เทคนิคจำแบบไม่ต้องท่อง (สไตล์พี่ปีโป้)
พี่ปีโป้แนะนำให้เรียงคิดตามลำดับนี้เสมอ
1️⃣ มี Hydrogen bond ไหม
2️⃣ ถ้าไม่มี ดู Dipole หรือไม่
3️⃣ ถ้ายังใกล้กัน ดูมวล + รูปร่าง
ถ้าคิดครบ 3 ชั้นนี้ ข้อสอบเรื่อง จุดเดือดไม่เท่ากัน แทบไม่พลาด
จุดเดือดไม่เท่ากัน สำคัญกับการสอบยังไง?
- ออกสอบ เคมี ม.ปลาย บ่อยมาก
- เชื่อมโยงกับเรื่อง
- แรงยึดเหนี่ยวระหว่างโมเลกุล
- สมบัติของสาร
- การแยกสาร (กลั่นลำดับส่วน)
ใครที่ยังสับสน มักจะพลาดคะแนนตรงบทนี้แบบน่าเสียดาย
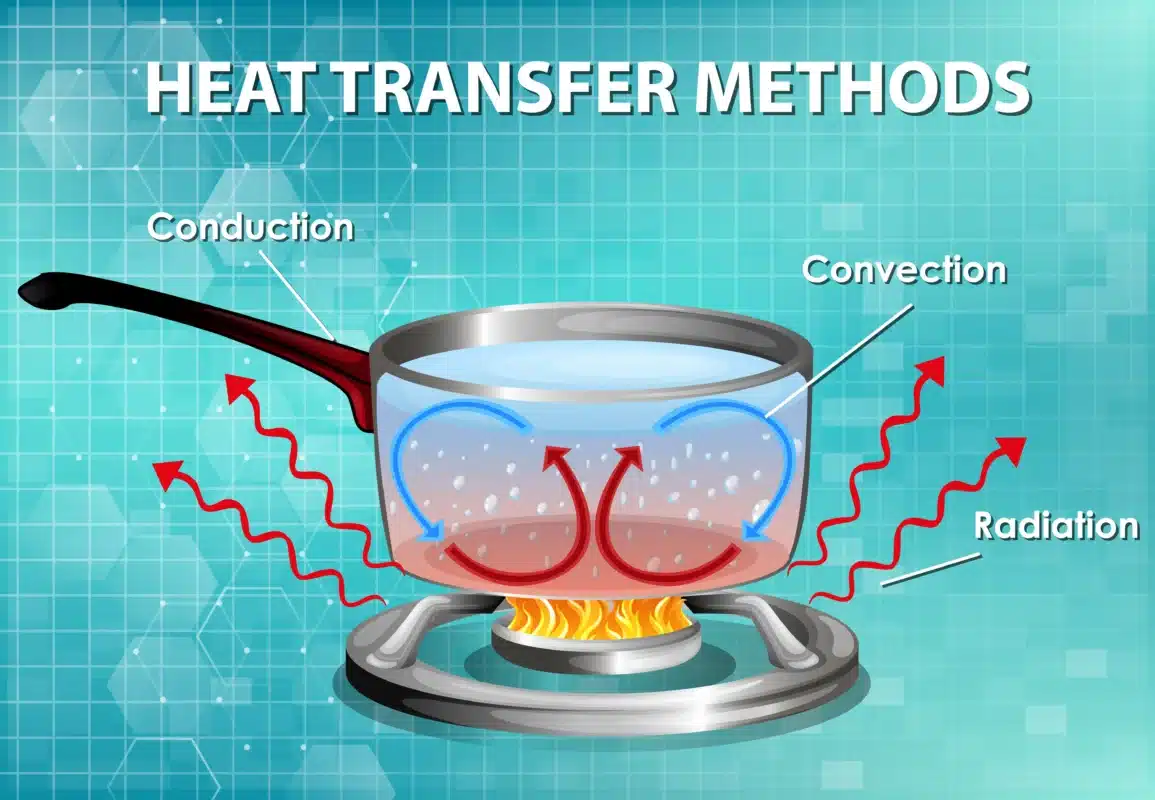
เรียนให้เข้าใจจริง ต้อง Kmepepo
ถ้าอยากเรียนเคมีแบบ “เข้าใจเหตุผล ไม่ใช่ท่องสูตร”
พี่ปีโป้แนะนำสถาบันติวเตอร์เคมี Kmepepo
จุดเด่นของ Kmepepo
- อธิบายเคมีจากพื้นฐาน → ระดับสอบแข่งขัน
- เน้นการคิดวิเคราะห์ ไม่ใช่จำอย่างเดียว
- เทคนิคทำโจทย์เร็ว ใช้ได้จริงในห้องสอบ
เหมาะมากสำหรับน้อง ๆ ที่อยากอัปคะแนนเคมี หรือเตรียมสอบสนามสำคัญ
FAQs: คำถามที่เจอบ่อยเรื่อง จุดเดือดไม่เท่ากัน
Q: สารที่มีมวลมากกว่า จุดเดือดสูงกว่าเสมอไหม?
A: ไม่เสมอ ต้องดูแรงยึดเหนี่ยวและโครงสร้างร่วมด้วย
Q: ทำไม H₂O จุดเดือดสูงกว่า H₂S มาก?
A: เพราะ H₂O มี Hydrogen bond แต่ H₂S ไม่มี
Q: ข้อสอบชอบถามแบบไหน?
A: เปรียบเทียบสารหลายชนิด แล้วถามว่าใครจุดเดือดสูงสุด พร้อมเหตุผล
Q: เรียนเองได้ไหม หรือควรเรียนติว?
A: เรียนเองได้ถ้าเข้าใจพื้นฐาน แต่ถ้าอยากเร็วและแม่น การเรียนกับติวเตอร์ช่วยประหยัดเวลามาก

